termodinamica química. problemas 1.- ¿cuántas calorías son necesarias para convertir 10,0 g de hielo a -15ºc en vapor de agua a 110ºc?. los
TERMODINAMICA QUÍMICA. Problemas
1.- ¿Cuántas calorías son necesarias para convertir 10,0 g de hielo a
-15ºC en vapor de agua a 110ºC?. Los calores específicos del hielo,
agua líquida y vapor de agua son, respectivamente 0,50; 1 y 0,5
cal/gºC. El calor de fusión del agua es 79,72 cal/g y el de
vaporización es 536 cal/g. (7,29 103 cal)
2.- ¿ Cuál será la cantidad de calor desprendida cuando 10 g de vapor
de agua a 100ºC se condensan y refrigeran hasta 5ºC?. Calor de
vaporización del agua 9710 cal/mol. (6340cal).
3.- Calcular el trabajo máximo realizado por 50,0 g de agua, cuando se
añaden, a temperatura constante, a una disolución de glucosa al 20 %.
La disolución está a 30ºC La presión de vapor de agua a 30ºC =31,824
Torr (25,5cal)
4.- Calcular el calor de reacción a 25ºC y 1 atm, del proceso:
, sabiendo que:
(284,98 kcal)
5.- Determinar el calor de formación de la cianamida, CH2N2, a partir
de su entalpía de combustión, cuyo valor es de -177,2 Kcal/mol y
conociendo los calores de formación del agua y del CO2 cuyos valores
son 68,32 y 93,97 Kcal/mol respectivamente. (-14,91 Kcal/mol)
6.- Calcular el calor de reacción en el proceso: C2H4+H2O C2H5OH
a 25ºC, conociendo los calores de combustión a 298K del alcohol
etílico, C2H5OH, y del etileno C2H4, que valen respectivamente 1367 y
1411 KJ (44 KJ)
7.- En la combustión del propano se desprenden 526,3 Kcal/mol.
Suponiendo que se aprovecha el 80% de esta energía ¿Cuántos Kgr de
agua a 15ºC se podrán convertir en vapor a 100ºC si se quema 1m3 de
propano medido en c.n.? Calor latente de vaporización 595,9 Kcal.
(27,61 Kg de agua)
8.- Cuando un mol de alcohol metílico, CH3OH, se quema, a 298ºC y a
volumen constante se desprenden 173,65 Kcal en forma de calor. ¿Cuál
es la ΔH para esta reacción? B) a 298 K el calor de formación del agua
líquida y CO2(g) son respectivamente, -68,32 y -94,05 Kcal. Calcular
la entalpía normal de formación del metanol líquido c) La entalpía de
vaporización del metanol es 8,43. Calcular la para el metanol
gas (-173,948 Kcal; b) -56,702 Kcal; -48,272 Kcal).
9.- El calor de formación del octano normal, C8H18, es de 60320
Cal/mol. Calcular la cantidad de calor desprendida en la combustión
completa de 10 g de n-octano, suponiendo que el gas formado queda en
estado de vapor. Si el calor se aprovecha en un 40% en calentar agua a
25C, hallar la cantidad de ésta que podrá transformarse en vapor a
100ºC. Los calores de formación del CO2 y del H2O en estado de vapor
son 94030 y 57800 cal. El calor específico del agua líquida es 1
cal/gºC y el calor latente de ebullición del agua 534,4 cal/g. (a)
106326,31 Cal; b) 69,2 .
10.- Conocidos los calores de combustión del etileno C2H4 (g), del
etano, C2H6(g) y del H2(g) a 25ºC y presión de 1 atm que son
respectivamente, -337,3; -372,8 Kcal /mol y -68,4 Kcal/mol, hallar el
calor de hidrogenación del etileno para dar etano. (-32,9 Kcal/mol)
12.- Hallar la energía de enlace H-Cl, sabiendo que la entalpía de
formación de HCl y las de disociación del H2 y del Cl2 son,
respectivamente, -92,3; 436 y 242,6 Kj/mol (431,6 Kj/mol).
13.- Calcular la variación de entalpía de la reacción de hidrogenación
del etileno para formar etano, sabiendo que las energías medias de
enlace son: C=C: 611; H-H: 436; C-C:347; C-H: 415 Kj/mol (-137 Kj)
14.- Hallar la variación de entropía que tiene lugar al fundirse 1 mol
de hielo a 0ºC y a la presión atmosférica. Calor latente de
vaporización = 79,72 cal/g (21,9 J/mol)
15.- Hallar la dS para una expansión reversible e isoterma de 1 mol de
un gas ideal desde 10 atm hasta 1 atm. (19,14 J/K)
16.- Hallar la variación de entropía en condiciones estándar que
corresponde a las reacciones: a) N2(g)+3H2(g) 2 NH3 (g). b) C(s)+H2O
CO(g)+ H2(g), sabiendo que la entropía molar estándar del NH3(g) =
192,5; N2(g) = 191,5; H2(g)=130,6; CO (g)=197,9; C(g)=5,73;
H2O(l)=70,0 J/mol K. Interpretar los resultados. (Sol: a) -198,3 J/K;
b) 252,8 J/K ).
17.- Será espontánea la reacción: N2O(g) N2(g) + ½ O2(g) si ΔHº =-
81,6 KJ; ΔSº= 75,3 J/K ( sol: si)
 BASES ESPECÍFIQUES I PARTICULARS DEL SERVEI DE JOVENTUT DE
BASES ESPECÍFIQUES I PARTICULARS DEL SERVEI DE JOVENTUT DE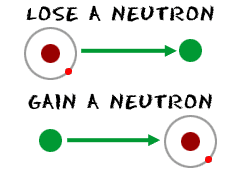 NAME DATE RADIO ACTIVE DECAY WEBQUEST
NAME DATE RADIO ACTIVE DECAY WEBQUEST ENGLISH DEPARTMENT DECLARATION OF ACADEMIC INTEGRITY I DECLARE THAT
ENGLISH DEPARTMENT DECLARATION OF ACADEMIC INTEGRITY I DECLARE THAT G ESCHWISTERSCHOLLGYMNASIUM PULHEIM QUALIMAPPE JUNIOR INFORMATIONSBLATT FÜR LEHRERINNEN UND
G ESCHWISTERSCHOLLGYMNASIUM PULHEIM QUALIMAPPE JUNIOR INFORMATIONSBLATT FÜR LEHRERINNEN UND Luleå Kommun 0 (1) 20050810 Luleå Kommun
Luleå Kommun 0 (1) 20050810 Luleå Kommun  FULL DE PARTIDA XÈ CAMPIONAT DE SCRABBLE DE XXXX
FULL DE PARTIDA XÈ CAMPIONAT DE SCRABBLE DE XXXX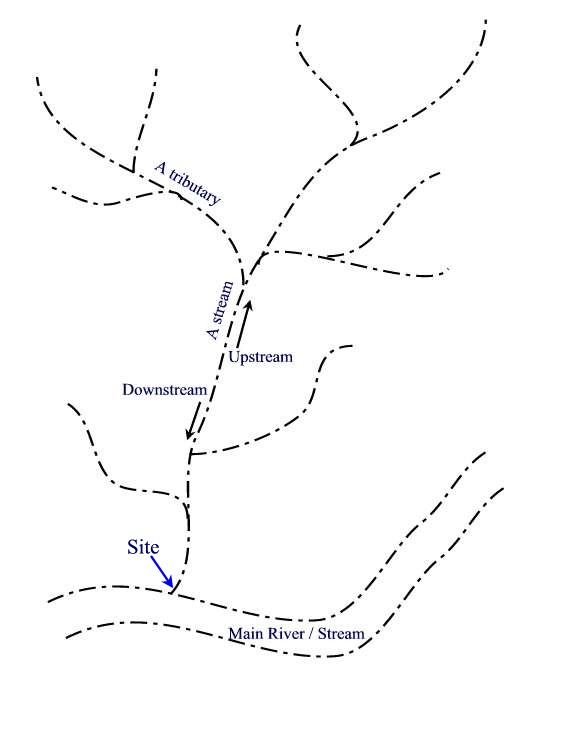 DRAINAGE AREAS AFTER A SITE HAS BEEN LOCATED
DRAINAGE AREAS AFTER A SITE HAS BEEN LOCATED SOLICITUD PARA LA PARTICIPACIÓN EN EL SORTEO DE PERMISOS
SOLICITUD PARA LA PARTICIPACIÓN EN EL SORTEO DE PERMISOS GOVERNMENT OF KARNATAKA SHIVAMOGGA INSTITUTE OF MEDICAL SCIENCES (AUTONOMOUS
GOVERNMENT OF KARNATAKA SHIVAMOGGA INSTITUTE OF MEDICAL SCIENCES (AUTONOMOUS HOME AND COMMUNITY BASED SERVICES MANUAL 900 APPENDIX
HOME AND COMMUNITY BASED SERVICES MANUAL 900 APPENDIX